關於人類抗衰老以及健康的科普知識。
1. 肝髒功能
肝髒是人類5大髒器之一,但是它與心髒,腎髒,肺部,腸胃相比,存在感並不強烈。大部分心髒疾病具突發性和致死性,讓人心生恐慌;腎髒與排尿、代謝、性功能息息相關,尿毒症,腎衰竭等腎髒疾病會對生活造成很多不便;肺部主管呼吸,還有吸煙這位勁敵存在,更加引人注意;腸胃不適,人體反應非常迅速,讓人難以忽視。
然而人們很少注意到肝髒,因為肝髒是唯一沒有痛感神經的器官,當人們發現肝髒出現問題的時候,很有可能已經是肝癌晚期了。
肝髒作為人體器官中“不愛哭沒糖吃的孩子”,雖然存在感低,但是它的功能卻是無與倫比的。肝髒是人體內最大的代謝器官,肝髒裏會發生700多種人體反應,合成蛋白質,合成糖原儲存能量,分解外界入侵人體的有毒物質,儲存人體95%的維生素A和其他維生素,是身體裏最大的鐵元素儲存站,產生專門溶解脂肪的消化液—膽汁。
2. NMN 與 肝髒健康
NMN在肝髒中的吸收
2011年,美國華盛頓大學對小鼠肝髒細胞NMN培養,小鼠肝髒細胞與人類極其相似,實驗結果顯示:肝髒細胞能夠吸收NMN並自主轉換成為NAD+ [1]。
NMN 與非酒精性肝病
非酒精性脂肪性肝病(NAFLD)是指不是由酒精損傷造成的,而是由其他因素致使肝細胞內脂肪過度沉積,最終形成的非酒精性脂肪性肝病。肥胖和胰島素抵抗是導致非酒精性脂肪性肝病的兩大大原因,該病在歐美發達地區和中國富裕地區患病率高達30%。
非酒精性脂肪性肝病會導致肝硬化,肝癌細胞複發,轉移,還有會引發二型糖尿病,動脈粥樣硬化等。
a. 缺乏NAD+ 有可能造成非酒精性肝病
2016年,中國第二軍醫大研究發現,人體缺乏NAD+是中老年人患非酒精性脂肪性肝病的重要原因。實驗發現:1, 年紀越大肝細胞內NAD+含量就越少,45歲之後肝細胞內的NAD+含量明顯下降。2. 缺乏NAD+的肝細胞內,胰島素抵抗現象和肝髒纖維化明顯上升,從而誘導了非酒精性脂肪性肝病。
b. 補充NMN 可緩解避免 NAD+缺乏引起的非酒精性肝病
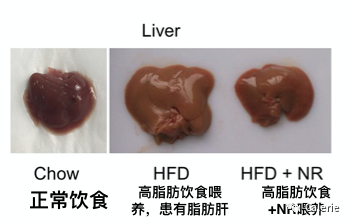
實驗的最後,科學家發現飲食中添加NAD+的前體補充劑, NR( 煙酸)幾乎完全糾正了小鼠肝髒的脂肪變性和脂肪性肝炎。而NR( 煙酸)在人體中第一步先合成NMN ,再合成NAD+,所以直接補充NMN是更加有效的方法。
實驗中,科學家用高脂肪食物喂養小鼠後,小鼠患有脂肪肝,肝髒肥大,在高脂肪飲食中添加NAD+前提補充劑,小鼠的脂肪肝情況明顯改善 [2]。
NMN 與酒精性肝病
a. 酒精肝成因及危害
酒精肝是由於長期大量飲酒所致的慢性肝病。初期通常表現為脂肪肝,進而可發展成酒精性肝炎、酒精性肝纖維化和酒精性肝硬化。酗酒者中約10%~20%有不同程度的酒精性肝病。酒精肝有可能直接導致硬化、肝腹水、肝性腦病、肝癌都有可能接踵而來,甚至還會出現肝昏迷和死亡等風險。
b. NMN在肝髒合成NAD+, 解酒護肝
人體攝入酒精後,其代謝途徑十分複雜,但是可以確定的是90%的酒精都要經由肝髒代謝處理,長期大量飲酒會對肝髒造成巨大的負擔。肝髒通過將乙醇分解為乙醛再分解為乙酸,最後形成二氧化碳和水排出體外,整個過程都需要大量NAD+的參與,NAD+的含量能直接影響肝髒解酒的速度和效率。如果酒精代謝緩慢產生酒精中毒,乙醛堆積,將會對肝髒造成巨大的損傷。
2018年,英國劍橋大學生物醫學院在《Nature》期刊發表論文,論文顯示,科學家發現飼喂患有酒精性肝病的小鼠NMN的第二天,小鼠體內的 NAD+含量明顯恢複,而NMN有效阻止了肝髒損傷的標誌物丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶的增加 [3]。
2019 年, 科學家們通過小鼠基因測序實驗發現,乙醇能夠誘變小鼠1778個基因,而NMN能夠有效保護437個 基因不受到乙醇的攻擊。人體攝入酒精後,其代謝途徑十分複雜,但是可以確定的是90%的酒精都要經由肝髒代謝 [4]。
引用文獻
[1] J. Yoshino, "Nicotinamide mononucleotide, a key NAD+ intermediate, treats the pathophysiology of diet- and age-induced diabetes in mice," cell metabolism, vol. 14, no. 4, pp. 528-536, 2011.
[2] C. Zhou, "Hepatic NAD+ deficiency as a therapeutic target for non‐alcoholic fatty liver disease in ageing," British Journal of Pharmacology, Vols. 2352-2368, 2018.
[3] J. I. Garaycoechea, "Alcohol and Endogenous Aldehydes Damage Chromosomes and Mutate Stem Cells," Natrue , vol. 533, no. 7687, pp. 171-177, 2018.
[4] M. A. Assiri, "Investigating RNA expression profiles altered by nicotinamide mononucleotide therapy in a chronic model of alcoholic liver disease," Human genomic, vol. 65, 2019.